Рак молочной железы - одно из самых распространенных, но в то же время и одно из наиболее успешно излечимых онкологических заболеваний. Шансы на победу над этой болезнью зачастую очень высоки - особенно если учесть современный уровень медицины, новые препараты, подходы. О том, как лечат рак молочной железы современные израильские врачи, мы поговорили с Ириной Живелюк - врачом высшей категории из израильской Sapir medical clinic.

Итак, у женщины появилось уплотнение в молочной железе, она прошла обследование, и подтвердился рак. Как действуют врачи дальше? Как формируют программу лечения, чем руководствуются?
Есть два основных параметра, которые определяют цели и тактику лечения рака молочной железы. В первую очередь это стадия опухоли, то есть, грубо говоря, сколько рака присутствует в организме. Второй фактор – тип опухоли. Ведь рак молочной железы – это не одно, а целая группа заболеваний. Существует, как минимум, 4–5 его разновидностей.
Существуют четыре основные стадии рака молочной железы. Первые три характеризуются различными размерами новообразования и наличием или отсутствием поражения лимфоузлов. В данном случае цель лечения – полностью избавить женщину от заболевания. Чем раньше установлен диагноз, тем выше шансы на успешный исход. Так, при первой стадии шанс выздороветь более 90%. При II и III стадиях шансы ниже, тем не менее, мы всегда стремимся к ремиссии.
Четвертая стадия – это рак с метастазами. В таких случаях цели лечения иные. Тут мы стремимся максимально затормозить прогрессирование болезни, не дать опухолевым клеткам так активно размножаться. И женщина зачастую может жить полноценной жизнью даже с болезнью.
Когда мы говорим о типе рака, то важно понимать, что есть опухоли более и менее агрессивные, чувствительные и нечувствительные к гормонам. И это тоже влияет на программу лечения.
Многим женщинам требуется и химиотерапия, и хирургическое лечение, и лучевая терапия. Многим показана только химиотерапия. В редких случаях удается обойтись только хирургическим вмешательством. Как правило, это пожилые женщины с очень небольшими опухолями. Всем остальным, кроме местного, лечения требуется системное, которое может включать классическую химиотерапию, гормональную терапию, таргетную терапию, иммунотерапию. Есть много классов противоопухолевых препаратов, их подбор зависит от размеров и типа опухоли.
Получить бесплатную консультацию по возможности лечения в Израиле рака молочной железы и других заболеваний, приобретению и доставки лекарств обращайтесь по e-mail: info@sapirmedical.com
Какими документами, протоколами руководствуются врачи при выборе лечения? Насколько жестко привязаны схемы лечения к стандартам? В какой степени нужно учитывать индивидуальные особенности женщины?
Зачастую в первую очередь мы должны определить тип опухоли, ее молекулярные характеристики. В этом помогает специальный анализ – иммуногистохимия.
Существуют определенные протоколы лечения. В них прописаны виды, дозы лекарств, режимы их приема, очередность применения разных видов лечения. Стандарты есть, но правильно лечить не опухоль, а конкретного пациента. Нужно учитывать возраст, сопутствующие заболевания, семейный анамнез и многие другие особенности. Мы должны решить, как максимально избавить женщину от опухоли существующими препаратами. Тут есть такое понятие, как максимально переносимая доза. Это такая самая высокая доза, которую можно дать человеку, не навредив ему.
Схема – это общее направление, которое врач должен подстраивать под конкретного пациента.
Среди женщин существует такая распространенная страшилка – «красная химиотерапия». Что это за схема лечения, как часто она применяется и насколько реально опасна?
В первую очередь нужно понимать, что любые химиопрепараты – это по сути яды, которые уничтожают опухолевые клетки. Их начали активно применять 30–40 лет назад, и за последние 20 лет не появилось ни одного нового химиопрепарата. Можно сказать, что самые хорошие химиопрепараты уже придуманы, и разработкой новых не занимается ни одна фармкомпания.
Красная химиотерапия тоже существует уже много лет. Это доксорубицин, эпирубицин и другие препараты, растворы которых имеют красный цвет. За последние годы препараты не поменялись. Но поменялось все, что касается поддерживающего лечения. Оно не дает химиопрепаратом вызывать тяжелые побочные эффекты. На сегодняшний день многие женщины переносят красную химиотерапию очень легко. Мало того, сейчас это одна из самых щадящих схем лечения при раке молочной железы. Сами химиопрепараты токсичны, но благодаря поддерживающему лечению сегодня от них уже никого не тошнит, не рвет, и из-за них не приходится постоянно лежать в постели.
Да, от красной химиотерапии выпадают волосы. Но это происходит и от любой другой химиотерапии при раке молочной железы.
Хорошо, в химиотерапии за последние десятилетия ничего не поменялось. А что изменилось за последние годы в методах лечения онкологических больных? Какие инновации появились? Чем может похвастать в этом плане израильская медицина?
В первую очередь изменились подходы к воздействию на опухоль. Раньше химиопрепаратами всегда пытались полностью уничтожить рак. В теории так можно и сделать: нагрузить организм максимальной дозой препарата, чтобы все раковые клетки погибли. Но химиотерапия влияет и на нормальные клетки организма, она токсична.
Поэтому в последнее время ученые создают новые препараты, которые влияют только на опухолевую ткань. Например, блокируют известные на данный момент факторы роста, которые заставляют раковые клетки размножаться. Либо препарат лишает клетку питания, и она погибает. Есть препараты, которые направляют опухолевую клетку в естественный путь гибели. Ведь в норме все клетки организма недолговечны – со временем они стареют, погибают. Опухолевые клетки лишены этого естественного механизма, и современные препараты помогают это исправить. Данные методы лечения неплохо работают.
Еще один современный тренд – иммунопрепараты. Они помогают организму определить опухолевые клетки как чужие и бороться с ними, примерно как с инфекцией. Иммунотерапия показывает высокую эффективность при ряде онкологических заболеваний, таких как рак легкого, кожи. При этих заболеваниях в опухолевых клетках много мутаций, и они очень непохожи на нормальные. Поэтому иммунную систему легко против них направить. При раке молочной железы опухолевые клетки, как правило, сильно похожи на нормальные, поэтому иммунитету их сложно распознать. К сожалению, здесь успехи иммунотерапии не так велики.
Таким образом, современные препараты направлены не на то, чтобы убить раковые клетки полностью. Вместо этого мы пытаемся затормозить их рост, активировать естественные механизмы старения и смерти. Это работает как дополнение к химиотерапии, и в современных схемах становится всё больше и больше препаратов.
Получить бесплатную консультацию по возможности лечения в Израиле рака молочной железы и других заболеваний, приобретению и доставки лекарств обращайтесь по e-mail: info@sapirmedical.com
А каковы современные принципы применения лучевой терапии при раке молочной железы?
Лучевая терапия применяется по двум показаниям. Паллиативная используется с целью облегчения состояния пациента при поздних стадиях рака. Излучение убивает опухолевые клетки, и женщина начинает чувствовать себя лучше. Например, исчезает боль, потому что опухоль перестает давить на определенный нерв.
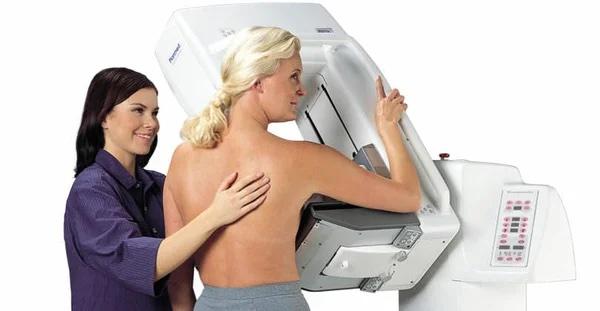
В 90% случаев при раке молочной железы применяют другой вид лучевой терапии – профилактическую. Суть лечения в большинстве случаев состоит в том, что злокачественную опухоль удаляют во время хирургического вмешательства, а оставшуюся ткань молочной железы облучают. Еще в 90-х годах онкологи стали постепенно уходить от удаления всей молочной железы. В ходе научных исследований на тысячах и десятках тысяч пациентов было доказано, что в большинстве случаев можно убрать только опухоль, затем облучить грудь, и это дает те же показатели выживаемости и смертности, как и операция по удалению всей молочной железы – мастэктомия. Прогноз не меняется.
Лучевая терапия по своему механизму и пути развития похожа на химиотерапию. Рентгеновские лучи были открыты много лет назад, и они давно применяются для борьбы с раком. Изменились только технологии. Во время облучения луч выходит из аппарата, проходит через всё тело пациента и останавливается только в свинцовой обшивке кабинета.
В последние годы изменилось планирование лучевой терапии. Это произошло благодаря развитию технологий, физики, математики и аппаратуры. Сегодня радиотерапию проводят с трех- и даже четырехмерным планированием. Выражаясь простым языком, это делают для того, чтобы облучить то, что нужно, и не облучить то, что не нужно. Раньше грудь облучали только из двух полей, и все ткани, находящиеся на пути лучей, получали примерно половину дозы. Сегодня физики умеют планировать облучение так, чтобы направить дозу точно на опухоль, почти не затрагивая здоровые ткани.
Учитываются и смещения опухоли во время дыхания. На вдохе молочная железа как бы выдвигается вперед, отходит от легких и сердца, а во время выдоха возвращается на место. Современные аппараты умеют облучать опухоль только в определенной фазе дыхания, и это не дает возможности причинить даже малейшего вреда соседним здоровым тканям. Такие аппараты называются линейными ускорителями, их производит несколько компаний, и все современные модели есть в Израиле. С помощью них врачи могут дать большую дозу на опухоль с минимальным вредом для здоровых тканей.
После хирургического лечения у некоторых женщин развивается такое осложнение, как лимфедема. Почему оно возникает, и можно ли что-то сделать, чтобы его предотвратить?
Лимфедема – это отек руки и грудной стенки, который может возникнуть после большой операции на подмышечной впадине.
Предотвратить это осложнение помогает правильное планирование операции. Например, если мы говорим о женщине, у которой поражены лимфатические узлы, и мы точно это установили – она никогда сразу не отправится на операционный стол. Сначала будет проведен курс химиотерапии, чтобы максимально, насколько возможно, уничтожить опухолевые клетки. Через несколько месяцев будет выполнена операция, и во время нее проводится сентинель-биопсия, или биопсия сторожевых лимфатических узлов.
Во время операции хирург вводит в молочную железу специальные «чернила» или изотопный препарат. Это помогает «прокрасить» лимфатические протоки и узлы. Лимфоузел, который прокрашивается первым – это то место, куда в первую очередь происходит отток лимфы от молочной железы и распространяются раковые клетки. Это может быть один лимфатический узел или несколько – их и называют сторожевыми. Если в сторожевых лимфоузлах нет раковых клеток, то и убирать все остальные нет смысла. Таким образом, убирают только сторожевые лимфоузлы, чтобы изучить под микроскопом, и лимфедемы после этого не бывает.
Если всё же пришлось удалить подмышечные лимфатические узлы, то больше чем у трети таких женщин рано или поздно возникнет лимфедема, и бороться с ней не получится. Эффективного лечения не существует. Массаж, физиопроцедуры, поддерживающее лечение, упражнения, – всё это помогает лишь в некоторой степени уменьшить отек и улучшить качество жизни. Во время операции пересекают лимфатические протоки, и из-за этого нарушается отток лимфы. Восстановить это уже не получится. Сейчас пытаются выполнять некоторые операции для устранения лимфедемы, но это направление пока еще только начинает развиваться. Единственный метод профилактики – предотвращать удаление лимфоузлов всегда, когда это возможно.
В чем отличия израильской медицины от медицины в других странах?
В Израиле нет такого понятия, как «врач лечит больного». В Израиле лечат больного всегда много врачей. Врачи, может быть, люди других специальностей, как психологи, физиотерапевты, неважно, но всегда несколько. Пациент — вот здесь, а вокруг него система. Поэтому мы всегда сидим с врачами-рентгенологами, с хирургами. Простого примера я вам скажу, у человека обнаружили что-то, взяли биопсию, нет рака. И я могу сказать, как хорошо, у тебя нет возврата болезни, у тебя биопсия чистая. Рентгенолог мне скажет: «Нет, это выглядит как возврат опухоли.
Значит сделали вторую биопсию, третью и четвертую, потому что я, как специалист в рентгенологии вижу это по-другому. Перепроверю еще раз, перепроверю еще раз». Плюс к этому мы сами, мы же тоже, несмотря на то, что мы израильская медицина, мы не считаем себя самыми умными. Бывают случаи, что мы консультируемся с докторами или со специалистами из других стран. Это, кстати, тоже очень принято. Написать известному доктору в этой области. У меня есть пациентка, короткие заключения, чтобы вы рекомендовали, и без всяких денег, и без всяких оплат, и все, тебе всегда ответят.
В Европе и в Америке есть комиссии, как у нас в Министерстве здравоохранения, у них в Америке есть FDA, комиссия. В Европе есть европейская комиссия по разрешению препаратов и технологий. Ни в Америке, ни в Европе ты не можешь это обойти. То есть лекарство, которое не зарегистрировано в Америке в FDA, человек получить не может. В Израиле лекарство, которое не зарегистрировано в Министерстве здравоохранения израильском, или технология, которая не зарегистрирована, для определенного пациента, если врач считает, что это нужно, врач должен это обосновать в Министерстве здравоохранения, и ты получаешь разрешение специфическое на этого пациента по номеру его паспорта.
То есть для этого требуется обоснование. То есть тебе нужно показать на основании чего ты думаешь, что это нужно. Это все делается через компьютер меньше, чем за 24 часа. Ты им посылаешь, там есть онлайн комиссия. Ты на следующий день получаешь, если это их убедило, ты получаешь разрешение. Когда мы облучаем женщинам грудь, даем им радиотерапию, в связи с анатомическим строением у нас молочная железа очень рядом находится с легкими, с сердцем и с органами важными, которые, к сожалению, луч ускорителя, он не знает, где. Тоже захватывает. Он останавливается в свинцовой стене. И технологии сегодня позволяют сделать это не только в трехмерном воображении, даже в четырехмерном, включая дыхание. То есть грубо говоря, когда женщина вдыхает, у нее грудная стенка отодвигается от сердца, и аппарат облучает только в момент, когда она на максимальном вдохе, и сразу выключается, когда она начинает выдыхать.
То есть не поражаются все ткани, которыми не нужно поражаться. Смысл облучения всегда, это не важно какой орган мы облучаем, это убить два качественные клетки, где нужно, и не поразить те, которые рядом. А к сожалению, дозы, которыми нужно убить два качественные клетки, они намного выше, чем дозы, которые поражают здоровые.
Соответственно, это влияет на уменьшение побочных явлений. Особенно, когда мы говорим о облучении каких-то опухолей в головном мозге, в глазу или в каких-то органах, где повредить другие структуры мы вообще не можем себе позволить. В Израиле очень распространено то, что называется «скрининг». То есть после определенного возраста мужчинам или женщинам предлагается довольно настойчиво делать определенный анализ. Например, женщинам после 50 лет всем два раза в год звонят и заставляют ходить делать маммографию. То есть не заставляют, а пока ты не придешь, то тебе будут звонить. Или там после 50 лет делать исследование кишечника, которое называется «кал на скрытую кровь» и колоноскопию. Они тебе будут звонить, звонить, звонить, пока ты не придешь. До чего это делается? Потому что, допустим, там, не знаю, маленький полип кишечника, который со 100% вероятностью переродится потом в рак, можно обнаружить тогда, когда он начал кровить и убрать, и рака не будет вообще.
Онкология сегодня это не онкология, которая была 20 лет назад. Большинство болезней, от которых раньше умирали очень быстро, распространенных стадий рака, сегодня люди продолжают жить с этой болезнью, естественно с лечением, жить с этим годами, как с хроническим заболеванием, как с диабетом люди живут. Как и с ВИЧ, в конце концов. Да, с ВИЧ, с диабетом люди живут, потому что есть лекарства. Тут абсолютно то же самое. Мы сегодня, если мы раньше давали только токсические препараты, как то, что называется химиотерапия, подавлять опухоль, пытаться их прибить. Сегодня большинство онкологий построено не на таких лекарствах, построено на препаратах, которые не дают клеткам опухоли размножаться с той скоростью, с которой они хотят. Или посылают клетки опухоли в сторону умирания.
Или, как есть сейчас такая область в онкологии, относительно новая, которая называется «иммунотерапия», это препараты, которые учат наш организм бороться с клетками опухоли, как будто они чужие, как с микробами. Онкология сегодня менее токсичная. Она более направлена на то, чтобы закрыть все механизмы роста, отправить клетку умирать. И люди живут с этими болезнями на самом деле годами. Годами, иногда даже десятилетиями. Не все об этом знают. Люди из многих стран едут, они сами об этом говорят, они едут за отношением.
Иногда приезжают пациенты, которые не понимают почему, не понимают, что. У них нет диалога, они не могут спросить, у них нет связи с доктором или с человеком, который может им объяснить. Мы сидим на первой встрече минимум час, на последующих между полчаса и часом, потому что вот эти встречи врача и пациента, кроме того, что надо посмотреть, послушать, он еще должен понять, что происходит, почему. И все абсолютно говорят: «Спасибо вам большое, что вы мне объяснили, потому что я уже год лечусь, и я вообще не понимаю, почему. Я где-то дочитываю в интернете, я где-то спрашиваю других». А это очень важно, потому что на основании этого сам пациент может принимать решение, что он будет делать, что он не будет делать, как он будет дальше планировать свою жизнь, потому что, к сожалению, не все пациенты могут излечиться. Это очень важно, и людям нужно об этом знать. Тем более, если они хотят, если они об этом спрашивают.
Стандарты лечения не только протоколы, что касается лекарств. Вообще стандарты лечения, подхода к лечению пациентов с онкологическими заболеваниями, они зависят от многих параметров: от стадии болезни, от вида болезни, и еще более таких, менее значимых. Каждый год эти стандарты обновляются официально в конце декабря. То есть все, что произошло нового, все, что себя доказало за тот год в мировой медицине, естественно, основываясь на научных работах, и потому что иначе невозможно. Мы не можем лечить людей, если я кого-то вылечила вот так, давайте будем всех так лечить, так это не работает. Стандарты мировых подходов и лечений к заваливанию обновляются раз в год, в конце декабря.
Если в середине года происходит какое-то научное открытие, или появляется лекарство, или появляется какая-то технология, или какой-то аппарат, скажем так, который делает, может быть, будет очень такое помпезное слово «переворот», но который делает резкий прорыв, то стандарты обновляются и в середине. То есть это не запланировано. Это происходит тогда, когда есть что-то «вау». Есть очень много препаратов в онкологии, которые мир стал употреблять не с конца декабря, 23 года, например, а с июня 23 года, потому что в июне это выяснилось. То есть в тот момент, когда мы знаем, что это делает какой-то важный толчок или важный прорыв в какой-то определенной области, это все можно начинать применять. Логистика всей этой, скажем, новизны, в Израиле она довольно легкая, скажем так. Потому что, как вы знаете, в любой стране, в России, в Америке, в Европе есть то, что называется регуляция. То, что называется Министерство здравоохранения. Реестр TrueFod, кодекс TrueFod.
Лекарств или технологий. Тот, кто одобрен в Министерстве здравоохранения. В Америке эта система называется FDA, то есть регистрация препаратов и продуктов, разрешенная к применению в стране. В тот момент, когда это зарегистрировано, можно принимать. В России есть Министерство здравоохранения, которое вносит раз, по-моему, тоже раз в год, потому что это невозможно делать чаще, с точки зрения администрации, новые препараты убирают старые препараты. В Израиле это контролирует Министерство здравоохранения.
Но чем Израиль отличается от большинства стран, что, если появилась, скажем, препарат лекарственный, он появился, он себя доказал, это научно обосновано, но он еще не зарегистрирован в Израиле, Израильское Министерство здравоохранения, то врач может обратиться напрямую в Министерство здравоохранения по поводу определенного пациента. Обратиться - это не как поговорить, это в электронном виде. То есть грубо говоря, послать электронное письмо в Министерство здравоохранения с обоснованием, почему он считает, нужно применить определенный препарат или определенную технологию, скажем, не знаю, гастроскопии или там операции какой-то.
И Министерство здравоохранения, если комиссия, которая посчитает, что обращение обосновано, то мы получаем разрешение на употребление определенного лекарства в течение 24 часов. Эта процедура очень простая и очень такая, скажем, не затягивающаяся, потому что это не занимает неделю, две или три. У нас даже есть пациенты, которые приезжают к нам из Америки, которые в медицине в общем-то считаются ведущими в мире. Когда им врачи там говорят: «Тебе нужно принимать определенное лекарство, я в Америке смогу тебе его начать давать только через месяц, потому что FDA его одобрит только через месяц. Но оно как бы стоит на одобрении FDA, но в Израиле ты уже можешь его получить, потому что там проще регуляция». Проще получить разрешение, естественно, его нужно обосновать.
Я как врач-онколог, о чем мы говорим последние годы очень много, что, если раньше, даже там 15-12 лет назад, онкологическое заболевание, распространенное, то, что называется «рак с метастазами четвертой стадии», это была болезнь, которая в общем-то считалась приговором. С появлением новых лекарств и новых технологий пациенты продолжали жить с этой болезнью дольше, то есть продолжительность жизни у них увеличилась, но, к сожалению, медицина не могла их вылечить. Последние годы в связи с очень бурным развитием фармакологии и бурным развитием компьютерной диагностики, появилось немало способов лечения, которые дают возможность человеку выздороветь от рака с метастазами, который в общем раньше был приговор.
Единственно, мы не говорим об этом как о рутине, к сожалению, пока. Я надеюсь, что на протяжении еще моей врачебной практики мы сможем на каком-то этапе говорить о излечении пациентов с метастазами, как о рутинном случае. Пока это те случаи, о которых вы спросили, то, что называется «интересный случай». То есть, когда сегодня мы можем подобрать препарат или технологию лечения пациенту по совокупности очень многих параметров, включая, кроме параметров самого человека, возраст, пол, история болезни, анамнез, включаем сегодня и параметры проверки опухолевых клеток, с одной стороны, на чувствительность или не чувствительность. Чаще мы проверяем на нечувствительность к определенным препаратам.
Когда мы можем проверить, насколько есть у организма определенного пациента резервов бороться с клетками опухоли, как с чем-то инородным. То есть, когда мы можем сегодня завести иммунную систему нашу, часть которой построена на войну с опухолевыми клетками у всех, у человека с момента, когда мы рождаемся. Но она, к сожалению, не у всех активна и не всегда умеет справляться с количеством опухолевых клеток. Сегодня мы умеем завести ее так, чтобы кроме лекарственных препаратов или какого-то инструментального метода лечения, мы можем завести иммунную систему так, чтобы сам организм начал убивать злокачественные клетки. И мы знаем, что после определенного промежутка приема препаратов, которые называются «иммунотерапия» в сегодняшнем языке, их можно прекратить употреблять, можно прекратить принимать, и организм будет дальше сам справляться с опухолью.
Уникальные случаи, если я могу сказать такое, что более понятно для людей, которые не связаны с медициной, есть такой вид рака, который называется «рак поджелудочной железы», который в общем-то один из самых таких, если вы заходите в Интернет, там написано, что это рак – один из самых плохих прогнозов, что большинство людей не живут больше чем год-полтора с этой болезни. Есть единичные пациенты, которые излечились. На наше удивление иногда. То есть естественно подход он такой, что мы хотим вылечить каждого. Но мы как врачи, мы знаем, что мы не можем вылечить всех. Но если мы не будем пытаться вылечить каждого, тогда мы не вылечим никого. Да, я как-то понятно говорю. То есть каждый пациент, который сидит напротив, я должна, как врач, употребить все свои знания для того, чтобы дать ему информацию, как минимум, о том, что сегодня есть в медицине мировой, максимально для того, чтобы он был здоров.
И эта возможность есть. Мир сейчас очень такой взаимосвязанный, скажем так. Если раньше было очень тяжело знать, что происходит в других странах, скажем, я уже не говорю там, в других больницах, в других странах. Сегодня, во-первых, мы все знаем, потому что все связаны, есть интернет, есть Конгрессы международные, которые, к нашему счастью, во время коронавируса перешли в виртуальную стадию. То есть для врачей это сделало огромный прорыв, потому что мы практически перестали ездить на Конгрессы физически. Потому что до коронавируса все новое, что узнавалось, оно в общем было представлено на Конгрессах. Врачи должны были туда лететь. Не все могли, не все могли на все эти форумы. После коронавируса мир научился, что мы можем слушать те же лекции виртуальные. Есть зумы, есть вебинары. Сейчас мы общаемся с врачами из других стран. По вечерам, во время ужина абсолютно спокойно. И оказалось, что это возможно, и это очень просто.
Если пациент из России решит лечиться в Израиле самыми современными препаратами – насколько легко или сложно организовать такой визит?
На сегодняшний день любой пациент из России может прилететь в Израиль и получить лечение. Есть много вариантов прямых перелетов и с пересадкой. Тем более. что со многими странами виза не нужна.
Сейчас Израиль - это прямой доступ к лучшим мировым методам лечения, лекарственным препаратам. Сейчас медицина в своем развитии шагнула очень далеко, поэтому нужно обращаться, искать варианты лечения.
Здоровья и мира всем!
Если у вас возникли вопросы к доктору Ирине Живелюк или хотите узнать о возможности консультации напишите на e-mail: info@sapirmedical.com
Помогаем с приобритением лекарств напрямую в израильских аптеках и доставкой до дома. E-mail: info@sapirmedical.com
